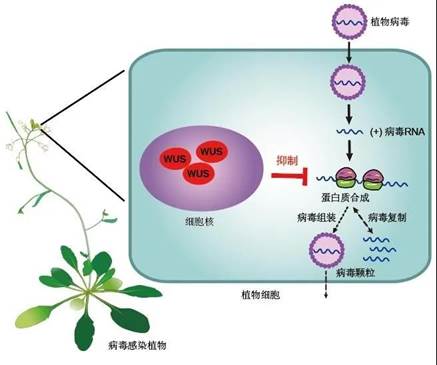
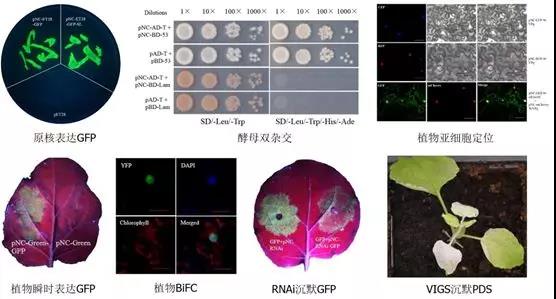
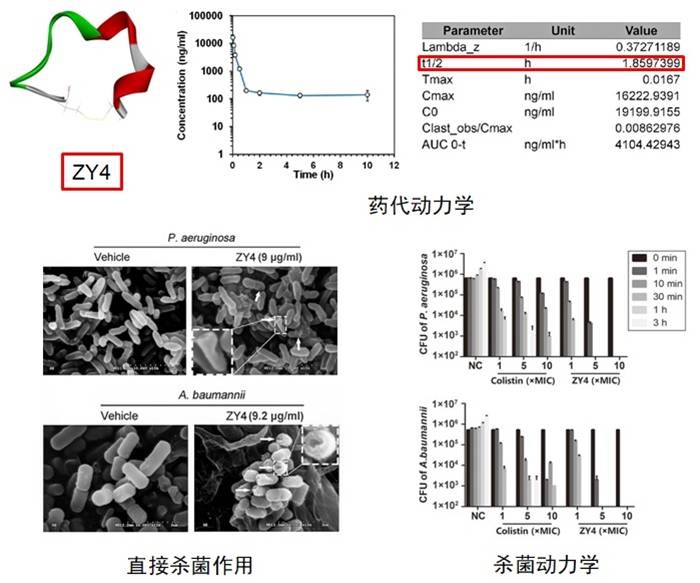
在城市的供水管道、蓄水池、冷却塔和空调系统中,隐藏着“危险分子”——嗜肺军团菌,该病菌会引起人体重症肺炎症状,俗称“空调肺”。当前,“狡猾”的嗜肺军团菌如“攻破”人类免疫系统,从而导致“空调肺”等疾病的过程,在科学界还未有清楚的认知。
近日,福建师范大学生命科学学院欧阳松应教授团队与普渡大学罗招庆课题组合作的一项研究,为深入探究嗜肺军团菌感染过程提供了线索。相关成果在国际著名期刊《欧洲分子生物学学会杂志》上发表。
“军团菌可不是普通的‘盗匪’,他们不仅擅长使用进攻武器“攻城拔寨”,同时还懂得如何有效合理地回收和恢复资源,保证军团菌长期可持续发展。我们的研究为大家展现了军团菌如何通过‘MvcA-MavC’这一对‘相互制约武器’,在感染过程中,利用其独特平衡机制,既不让免疫系统伤及细菌本身又不至于因为持续抑制免疫反应,而导致寄主细胞死亡影响病菌繁殖。”欧阳松应说。
病菌“进攻”也需要掌握一个“度”
在日常生活中,我们要面临各种病原微生物的威胁,军团菌就是其中之一。
据了解,当前现已分离了超过30种军团杆菌,至少19种是人类肺炎的病原,其中最常见的为嗜肺军团菌,占病例的85%~90%。我国于1982年在南京首次发现该病菌,此后在北京、上海等城市陆续发现。
“病原微生物与人类之间进行着长期而复杂的斗争,病原微生物通过不断繁殖、变异和进化,增强自己的毒力或致病力。病原体侵入人体后,人体就是病原体生存的场所,医学上称为病原体的宿主。”欧阳松应补充说,不过,人体或动物不像人工培养细菌的培养基,可以让病菌不受限制地肆意生长繁殖,轻易地导致机体死亡。病原体入侵后,机体强大的免疫系统能够消灭、排出、战胜入侵的病原微生物。
“泛素化修饰能够调控真核细胞中几乎所有的过程,尤其在细胞分裂和免疫反应等方面起不可或缺的作用。”欧阳松应介绍说,许多病原菌在与宿主细胞的长期博弈过程中,进化出多种方式来干预宿主的泛素修饰系统,从而达到增强侵染效率和逃避宿主免疫“监视”的目的。
“嗜肺军团菌主要通过一个称为Dot/Icm的IV型分泌系统,分泌大约330个效应蛋白“武器”到宿主细胞中,‘挟持’和‘干扰’宿主的各种信号通路,抑制机体的免疫系统,以辅助细菌在宿主细胞内的增殖。”欧阳松应说。
欧阳松应指出,需要注意的是,嗜肺军团菌能够成功感染宿主,需要掌握一个“度”:这些“武器”需要既能够劫持并抑制宿主的免疫系统完成感染,同时又不能因为过分抑制而导致机体免疫力下降过多而引起细胞死亡,失去赖以生存的“寄居所”。
这对“武器”是病菌的保持平衡的秘诀
在宿主的免疫反应和细胞生存等过程中,有个不能忽视的重要“角色”——UBE2N。
欧阳教授的合作伙伴,美国普渡大学教授罗招庆在前期研究中发现,嗜肺军团菌的效应蛋白MavC通过一定的催化方式将泛素(Ub)连接到UNE2N上形成UBE2N-Ub,从而完成对UBE2N的泛素化修饰并抑制其功能。持续抑制UBE2N的功能,会降低机体的免疫力,导致感染细胞死亡,不利于军团菌在胞内的增殖。
那么嗜肺军团菌通过谁来逆转这个抑制过程,完成这个平衡过程呢?科技日报记者了解到,在最新的这项研究中,他们给出了答案。
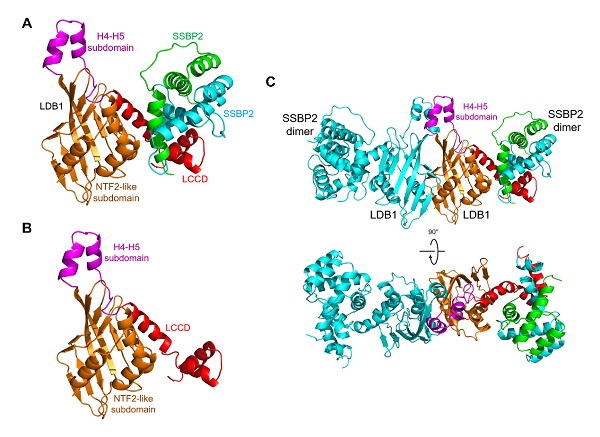
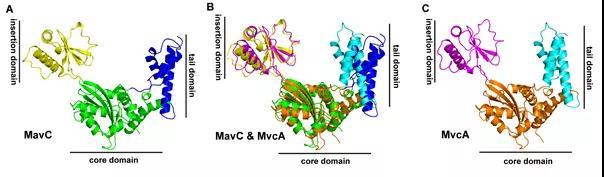
“我们在研究中发现,位于嗜肺军团菌的效应蛋白MavC下游的MvcA基因,编码了一个能特异性地对UBE2N-Ub进行去泛素修饰的酶——MvcA。令人意外的是,MvcA和MavC在蛋白序列和结构上高度相似,且均具有泛素脱酰胺酶功能。”欧阳松应说。
“如果把嗜肺军团菌比喻为‘盗匪’头目的话,该发现就好比‘盗匪’头目,派了‘俩小偷’MavC 和MvcA互相配合,偷盗前,MavC负责蒙蔽UBE2N,从而更容易控制宿主。5小时后,MvcA负责释放宿主,而后恢复UBE2N的功能。”欧阳松应教授比喻说。
由此表明,嗜肺军团菌通过控制MavC和MvcA在感染过程中的表达,满足在不同时间段平衡感染细胞对UBE2N功能的需求。
据悉,这是继欧阳松应课题组于今年7月在国际顶级期刊《自然》主刊上发表嗜肺军团菌相关研究以来的又一重大进展。该研究不仅揭示了谷酰胺脱氨酶―MvcA的全新功能及其催化机制,更为重要的是,也为探究两个蛋白质结构高度相似,但生化功能截然的原因提供了线索,也为临床治疗“空调肺”药物开发提供了新方向。(记者 谢开飞 通讯员 李玉莲)